这个用来救命的东东要召回!家里有过敏患者的要注意了!
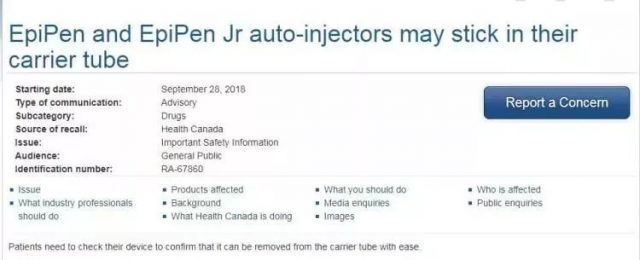
由加拿大生产的过敏患者紧急使用的两款肾上腺素自动注射器EpiPen和EpiPen Jr,因包装问题被卫生部召回。
召回产品:
0.3 毫克EpiPen ,药物识别号码(DIN)为00509558,有效期为2018年4月至2019年10月;
0.15毫克EpiPen Jr,DIN为00578657,有效期也是2018年4月至2019年10月。
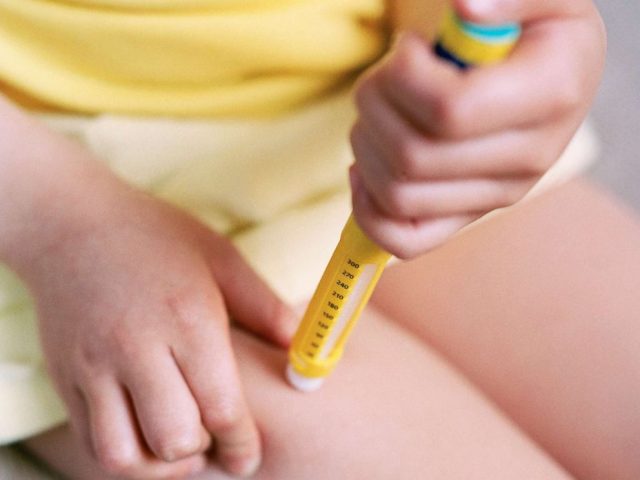
EpiPen作为一种肾上腺素自动注射器,具有很好的急救疗效,很多过敏患者都随身携带该注射器。此次被召回的两款EpiPen因包装存在问题,EpiPen很难从便携管中取出,在危机时刻很可能耽误或妨碍治疗,故被卫生部召回。
据悉,生产该注射器的加拿大公司——加拿大辉瑞制药公司(Pfizer Canada)尚未召回问题产品,该公司表示被召回的EpiPen仅是出现少数标签粘贴不当问题或标签黏住便携管的问题。他们已经请专业人士测试药品是否可以正常使用。
据美国CNN报道,继22个国家召回了缬沙坦(Valsartan),美国食品和药物管理局(FDA)于7月也发布了召回公告。
究竟缬沙坦(Valsartan)是种什么药物,为什么这么多国家对它如临大敌呢?
美国公布召回的Valsartan药品来源
据FAD解释,缬沙坦(Valsartan)是一种用于控制血压和预防心力衰竭的常用药物,因为该药物含有一种潜在致癌风险的化学物质,因此对它进行召回。
缬沙坦(Valsartan)不受专利限制,可用于其他仿制药的成分,但并非所有含该成分的药物都被召回。
美国公布的本次召回的药品包括以下几款:
药品名:Valsartan
生产公司: Major Pharmaceuticals
药品名:Valsartan
生产公司: Solco Healthcare
药品名:Valsartan
生产公司: Teva Pharmaceuticals Industries Ltd
药品名:Valsartan / Hydrochlorothiazide (HCTZ)
销售公司: Solco Healthcare
药品名: Valsartan / Hydrochlorothiazide (HCTZ)
销售公司: Teva Pharmaceuticals Industries Ltd
为什么只有这些药品被召回呢?
FDA药物评估和研究中心主任Janet Woodcock解释,
“我们仔细评估了在美国销售的含缬沙坦(valsartan)的药物,我们发现上述公司生产和销售的valsartan不符合我们的安全标准。这就是我们要求立即召回这些公司的产品,并立即采取措施保护患者的原因。”
最早开发这种药物的 Novartis公司表示,Sandoz valsartan 和 valsartan/ HCT 薄膜片正在欧洲和亚洲被召回,因为它们“不符合我们的高质量标准”。
该公司已经建议英国药店召回含有Dexcel Pharma Ltd和Accord Healthcare两家公司制造药物成分的缬沙坦(valsartan)批次。
根据FDA的声明,召回的深层次原因是存在被召回产品中发现的杂质N-亚硝基二甲胺(NDMA)。
终于搞明白了,原来有问题的不是valsartan,而是valsartan中含有了杂质。
这个杂质NDMA究竟是什么东东?
NDMA是一种强效致癌的有机化学物质。它被用于制造液体火箭燃料,软化剂和润滑剂等产品。
它也可以通过某些化学反应而不经意的产生,也是生产农药、橡胶轮胎或鱼类加工时的副产品。
根据动物医学研究表明,NDMA可能有毒并导致肝脏、肾脏和呼吸道肿瘤。
一定剂量的NDMA会对人体也会产生潜在伤害。
根据美国卫生和公共服务部的数据,接触高含量的NDMA会导致肝损伤,可能成为一种人类致癌物。
国际癌症研究所(IARC)把它列为2A级的致癌物。
NDMA的致癌风险有多大?
Novartis公司发言人Eric Althoff在上周首次召回后表示,在美国销售的产品并未受到此次召回的影响。
但FDA正在进行的审查和实验室检测中发现了其他情况。
FDA声称,NDMA的存在是出乎意料的,并且可能导致药品成分发生变化。
Althoff在7月6日的一封电子邮件中提到,“在Valsartan API中发现的NDMA数量远低于NDMA的累积的内源性产量和通常的外部暴露量。
这种杂质可能导致癌症的风险程度尚不确定。
因此,缬沙坦API中发现的NDMA数量并不代表服用Sandoz Valsartan和Sandoz Valsartan HCT薄膜片患者的致癌风险会显著增加。“
虽然如此,但是FDA对该药物的调查仍在继续。
FDA行政长官Scott Gottlieb博士当天表示。
“当我们发现药物质量和生产环节出现的失误有可能给患者带来风险时,我们全力以赴采取紧急行动提醒公众,并帮助有关单位从市场上移除这些药品。
今天在我们去召回这些既定药品的同时,我们的医疗药品供应团队也正在努力提供足够的、未受影响的药品来确保在全美范围内满足患者的治疗需求。
FDA致力于维护我们安全性和有效性的黄金标准。这包括我们努力确保药品质量和安全生产. “
加拿大采取相关行动
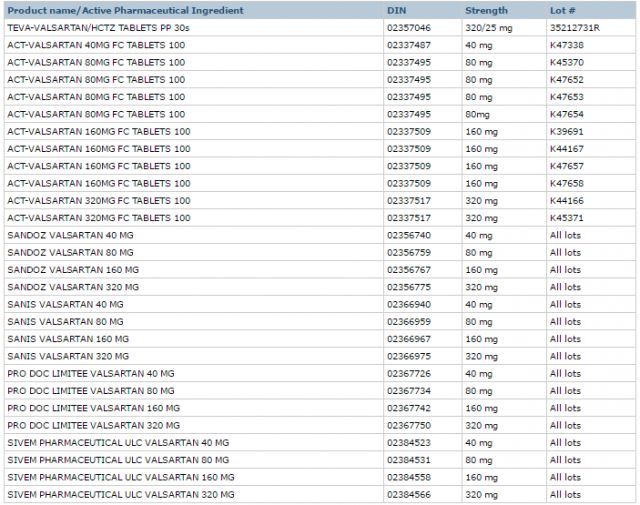
加拿大卫生部列出的一系列被召回的药品如下,一共28款。见下图。
高血压、心脏病患者该怎么办?
如果您或者您的家人正在服用这些被召回的药品,应尽快咨询医生,寻求专业指导意见。
未经医生允许,高血压、心脏病患者不应停止服用药物。
美国心脏协会提示,在没有监护的情况下停药,患者可能会更加危险。
卫生部建议,消费者可以测试便携管是否能够打开并轻易取出EpiPen,只要不在取出时释放药剂就没有问题。如发现不能取出请立即更换产品。