
FDA批准更新版新冠疫苗 两款均对EG.5有效
周一,食品和药物管理局(FDA)批准了Moderna和辉瑞/BioNTech两家公司更新后的新冠疫苗加强针。更新后的疫苗均已批准用于12岁及以上人群,并授权在紧急情况下供6个月至11岁人群使用。作为FDA更新的一部分,Moderna和辉瑞/BioNTech原先的二价新冠疫苗已不再被授权在美国使用。
FDA生物制品评估和研究中心主任彼得·马克斯(Peter Marks)在周一的发布会上说:“疫苗接种对于公共卫生和持续预防新冠病毒造成的住院和死亡等严重后果依然至关重要。公众可以放心,这些更新的疫苗符合本机构在安全性、有效性和生产质量方面的严格科学标准。我们非常鼓励那些有资格的人考虑接种疫苗。”
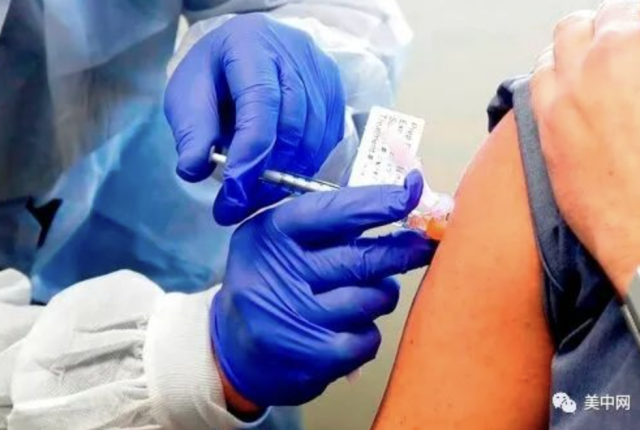
Moderna和辉瑞/BioNTech两家疫苗制造商均表示,测试结果表明他们的疫苗对于美国目前的主要毒株EG.5有效。
在FDA批准之后,由独立专家组成的免疫实践咨询委员会将会权衡更新疫苗的安全性和有效性,并向疾病控制和预防中心(CDC)给出疫苗接种的决策建议。而在CDC主任签署相关建议后,更新后的新冠疫苗即可展开接种工作。
另据CNN报道,FDA的最新决定是在近期新冠病例再次攀升之后做出的。目前,大多数6个月以上的美国人都有资格接种本季新冠疫苗。FDA则表示,无论此前是否接种过疫苗,5岁及以上者都有资格在最后一次接种新冠疫苗至少2个月后接种更新后的单剂疫苗。
去年10月,辉瑞公司在投资者电话会议上曾表示,更新后的新冠疫苗定价会在每剂110元至130元之间。
根据《可负担医疗法》,大多数保险计划都涵盖接种新冠疫苗的全部费用。没有保险或保险不足的人士则可通过CDC的“桥梁接入计划”(Bridge Access Program)获得免费的更新疫苗,但该计划将于2024年12月停止。






