首項結果!用瑞德西韋後68%新冠病人好轉 在華重症研究終止
備受關注的瑞德西韋(Remdesivir)治療新冠肺炎的首個臨床研究結果4月10日公布。在53名來自全球的患者中,36人(約佔68%)獲得了臨床改善。
瑞德西韋是一款在研藥物,前期主要用於治療埃博拉和中東呼吸綜合征等疾病,目前還未在全球任何一個國家獲批上市。
此前,美國首例新冠肺炎確診患者在接受了瑞德西韋治療後癥狀出現了立竿見影的改善,隨後該葯受到廣泛關注。

吉利德科學3月份提供的在美國製造的瑞德西韋的照片。(圖片來源:吉利德科學/美聯社)
53名來自全球的患者接受同情用藥,非臨床試驗
上海澎湃新聞報道,吉利德科學公司(Gilead Sciences)10日在頂級醫學期刊《新英格蘭醫學雜誌》(NEJM)上發布了瑞德西韋治療新冠肺炎(COVID-19)的首個臨床研究結果。
研究顯示,53名新型冠狀病毒肺炎嚴重併發症的住院患者,以個例同情用藥的方式接受了在研抗病毒藥物瑞德西韋的治療。這53名來自全球的患者中,36人(約佔68%)獲得了臨床改善。
值得注意的是,在首批公布的臨床數據中,總計32名患者(約佔60%)出現副作用,最常見的是肝臟酶指標升高、腹瀉、皮疹、腎功能障礙和高血壓。
總計12名(23%)患者出現嚴重副作用,其中包括多器官多器官功能障礙綜合征、敗血性休克、急性腎臟損傷和高血壓。
另外,接受治療的53名患者中,有7名在完成瑞德西韋治療後死亡,其中包括6名接受有創通氣的患者和1名接受無創氧氣支持的患者。
上述結果公布以後,引發業界的討論。有一種觀點認為,由於樣本數據量過小,且無對照組數據,這一結果的實際意義值得商榷。
吉利德科學11日在中國官網公布了該公司董事長兼首席執行官丹尼爾·奧戴(Daniel O』Day)的公開信。
信中說,這些患者是無法參加臨床試驗的危重患者,通過同情用藥程序,他們接受了瑞德西韋的治療。單純從研究角度來看,這些同情用藥的數據存在局限性,
然而,這些數據對於獲得了癥狀改善的患者來說有著非常大的意義。這53名患者的早期數據並非通過臨床試驗獲得,且數據只覆蓋了少數接受瑞德西韋治療的危重患者。
人民日報健康客戶端報道,北京醫院藥學部副主任藥師張亞同介紹:「同情用藥是允許給一些不符合批准的臨床條件,但無藥可救的患者,在開展臨床試驗時,使用尚未得到批准上市的藥物。」
在中國進行的一系列研究中,新冠重症患者的死亡率在17%-78%之間,與這些數字相比,該研究提供了瑞德西韋治療重症患者13%的死亡率的最新數據,值得關注。
張亞同稱,對於瑞德西韋有效性及安全性研究,有待進一步臨床研究。
全球共有7項研究 中國針對重症患者的研究已停止
丹尼爾·奧戴的公開信中透露,中國針對重症患者的研究已停止。
關於臨床試驗,信中說,有7項臨床試驗已經啟動。中國在2月初啟動了最早的兩項對重症和中症患者的研究。此後,新增的5項試驗在世界各地啟動。
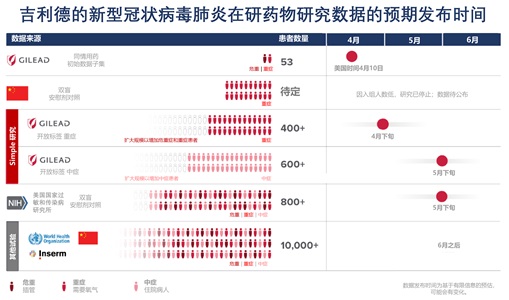
瑞德西韋各項試驗的匯總和預期的數據公布時間。(圖片來源:吉利德科學官網)
吉利德正在美國、亞洲和歐洲的新型冠狀病毒肺炎高發地區進行兩項三期研究。其中一項研究針對重症患者,另一項研究針對中症患者。
美國國家過敏和傳染病研究所(NIAID)於2月21日開始了一項全球試驗。該試驗將隨機分配患者使用瑞德西韋或安慰劑,以對照比較試驗結果。該試驗正在入組約800名具有不同癥狀的患者。
世界衛生組織也在進行一項全球試驗,名為Solidarity,Inserm DisCoVeRy試驗最近已在歐洲開始。
信中透露,預計在4月底獲得瑞德西韋針對重症患者研究的初步數據。中國的研究者將負責發布瑞德西韋在中國的試驗數據,
但是,因入組停滯,針對重症患者的研究已停止。預計5月份獲得有安慰劑對照的NIAID試驗的初步數據,以及吉利德的針對中度癥狀新型冠狀病毒肺炎患者的研究數據。