美國新冠疫苗進入臨床試驗 中國5條技術路線推進
目前,全球多種疫苗路線正齊頭並進,中國沿著5條技術路線加速疫苗攻關工作。而美國生物技術公司Moderna官方5日宣稱,食品藥品監督管理局(FDA)已完成對該公司研製的新型冠狀病毒mRNA疫苗——「mRNA-1273」的審查,批准其進入臨床試驗。
北京《科技日報》9日消息,據媒體稍早時間報道,Moderna公司最初預計,mRNA疫苗的研發可能需要三個半月以上,不過,研發組多達100名的科研人員進度非常快,從病毒基因組測序到發布疫苗僅用了42天,Moderna公司首席技術運營和質量官胡安·安德烈斯表示,這是應對全球衛生緊急情況下「創紀錄的速度」。
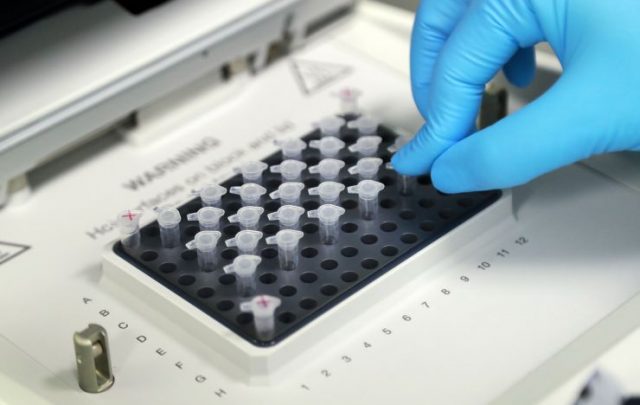
2月1日,中國科研人員展示新型冠狀病毒mRNA疫苗研發實驗過程。(圖片來源:中新社)
自上個月底,作為上市藥商的Moderna宣布其新冠病毒疫苗的消息後,該公司股價一路飆升,消息稱投資者對其第一批疫苗感到興奮。
將由健康志願者進行藥物測試
通常,信使核糖核酸(mRNA)疫苗是在體外合成病毒的相關序列mRNA,再將mRNA傳遞到人體細胞內形成免疫記憶。據Moderna公司表示,「mRNA-1273」疫苗即是抗新型冠狀病毒的mRNA疫苗,可針對病毒的刺突蛋白髮揮作用。而刺突蛋白,正是病毒感染宿主細胞的關鍵所在。
2月24日,「mRNA-1273」的第一批人體疫苗,已被運送至位於馬里蘭州的美國國立衛生研究院(NIH),由NIH接收,用於第一階段臨床試驗。
在FDA批准「mRNA-1273」疫苗進入臨床試驗後,Moderna公司開始招募45名健康志願者進行藥物測試,具體結果或將於7月或8月宣布。
是否進行動物實驗尚不清楚
此次,美國從基因測序到FDA批准疫苗臨床試驗進展如此之快,令人咂舌。那麼在FDA批准臨床試驗之前,Moderna公司有進行動物實驗嗎?
科技日報記者為此採訪了中國康希諾生物股份公司董事長宇學峰博士,康希諾生物在世界範圍內提供預防傳染病和感染病的解決方案,並專業從事高質量人用疫苗研發。
宇學峰博士表示,從目前掌握的資料來看還不清楚。按照疫苗研發的常規,動物實驗是必需的環節,一般是要建立動物模型,檢驗候選疫苗的免疫原性和對動物的保護性,在臨床試驗前,動物的安全性毒理實驗也是必需的。鑒於報道說臨床試驗在4月底前進行,目前動物實驗是否在進行中尚不了解。
值得注意的是,新冠疫情暴發之後,中國科學家快速確定了新冠病毒的全基因組序列,並於1月11日與世界衛生組織分享這一信息,幫助了全球科研機構研發藥物。Moderna公司和NIH下屬國家過敏和傳染病研究所(NIAID),正是第一時間分析了該病毒基因組序列,找到了他們認為最有可能在疫苗中產生預期免疫反應的部分。
在3月6日召開的新聞發布會上,中國國家衛健委醫藥衛生科技發展研究中心主任鄭忠偉表示,中國現在沿著5條技術路線推進疫苗攻關工作,包括滅活疫苗、基因工程重組亞單位疫苗、腺病毒載體疫苗、減毒流感病毒載體疫苗、核酸疫苗。綜合起來講,目前5條技術路線都在穩步推進。估計到4月份,按照中國有關法律法規規定,部分疫苗有希望進入臨床或者應急使用。