
兩款新冠疫苗已開展臨床試驗,大規模使用得到明年底
本周,一款名為INO-4800的新冠病毒疫苗開始進行一期臨床試驗,至此美國已有兩款新冠病毒疫苗開展一期臨床試驗。官員和專家表示,美國從研發疫苗到開展一期臨床試驗的速度創下紀錄,但即便一切順利,疫苗大規模投入使用可能也要等到2021年底。
美國開展臨床試驗的第一款疫苗是mRNA-1273疫苗,由美國國家過敏症和傳染病研究所和莫德納公司合作研發。mRNA-1273是一種信使核糖核酸(mRNA)疫苗,可針對病毒的刺突蛋白髮揮作用。刺突蛋白是病毒感染宿主細胞的關鍵所在,也是過去研發嚴重急性呼吸綜合征(SARS)冠狀病毒疫苗和中東呼吸綜合征(MERS)冠狀病毒疫苗時的靶點。
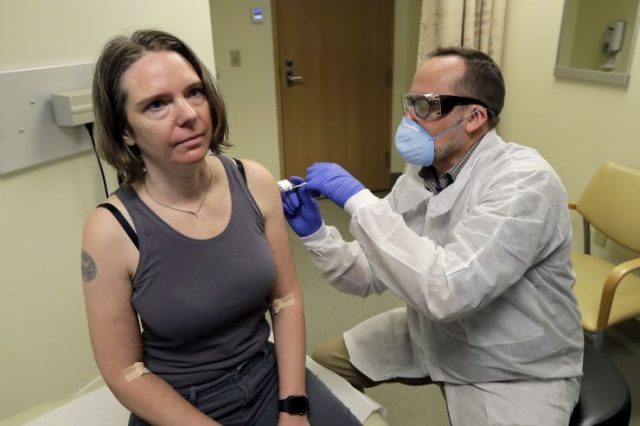
Jennifer Haller(左)16日在西雅圖接受首支試驗性新冠病毒疫苗注射。(圖片來源:美聯社)
傳統疫苗通常使用滅活病毒方式研製,而mRNA-1273疫苗是由體外合成病毒相關mRNA序列研發而成。3月16日,mRNA-1273疫苗的臨床試驗在位於西雅圖的凱撒醫療集團華盛頓衛生研究所開始實施。莫德納公司表示,從選擇疫苗的mRNA序列到首名志願者完成疫苗注射只花了63天。
按計劃,45名年齡在18歲至55歲之間的健康志願者參與mRNA-1273疫苗一期臨床試驗,接受間隔約28天的兩次疫苗手臂肌肉注射。他們分為3組,接受注射劑量分別為每次25微克、100微克和250微克,以便評估不同劑量的安全性以及其激發人體免疫反應的能力。志願者在完成兩次疫苗注射後將接受為期一年的觀察。
INO-4800疫苗由美國伊諾維奧製藥公司研發,是一種DNA(脫氧核糖核酸)疫苗,使用了被稱為質粒的一小段病毒環狀DNA片段,注射後能使細胞產生病毒的蛋白,從而激發免疫反應,安全性和可靠性較高。
4月6日,INO-4800疫苗一期臨床試驗在位於費城的賓夕法尼亞大學醫學院和位於堪薩斯城的藥物研究中心同時展開,共有40名成年健康志願者參與。志願者將間隔4周接受兩劑疫苗注射。伊諾維奧製藥公司表示,疫苗安全性及其激發的免疫反應等數據預計在今年夏末公布。
多名美國專家在接受新華社記者採訪時強調,疫苗進入一期臨床試驗的門檻並不高,但評估其安全性和有效性會持續相當長時間,樂觀估計疫苗大規模投入使用也要等到2021年底。
加利福尼亞大學聖迭戈分校傳染病系主任羅伯特·斯庫利說,候選疫苗進入一期臨床試驗相對容易,需要滿足的條件是能夠將病毒蛋白送入免疫系統的關鍵部位,使免疫系統能識別病毒,這可通過使用病毒蛋白、滅活或減活病毒、病毒RNA或DNA實現。
斯庫利說,在一期和二期臨床試驗對候選疫苗的安全性、其誘導的免疫反應進行評估後,效果顯著的疫苗將進入規模較大的三期臨床試驗,評估其降低感染率和致病嚴重程度的有效性,這個時間通常需要一年以上。
斯庫利說,疫苗從開始研發到美國食品和藥物管理局批准上市,整個過程通常需要兩年以上時間,具體時長取決於病毒傳播的嚴重程度和疫苗試驗的有效性。病毒感染率越高,疫苗試驗效果越好,其審批時間越短。
隨著白宮8日批准佛蒙特州進入「重大災難狀態」,美國新冠肺炎的「災情」地圖已擴大到至少45個州以及首都華盛頓特區。
據美國約翰斯·霍普金斯大學8日晚10時數據,美國已有超過43.2萬人感染新冠肺炎,死亡14817人。其中紐約確診15.1萬人、新澤西確診4.7萬人、密歇根確診2萬人、加利福尼亞確診1.8萬人。
中新社報道,總統特朗普8日在白宮發布會上表示,從5月份開始,美國將有約3億隻口罩陸續交付,並將根據需要再額外訂購2億隻作為儲備。截至8日,美國政府已分發逾8000台呼吸機,另有1萬台準備交付。
對於何時重啟經濟,特朗普表示,必須等到疫情曲線處於明顯下行區間,屆時將根據衛生專家等專業人士意見作出決定。






